Informe técnico: Virus de la influenza aviar A (H5N1) altamente patógena
Actualizado el 7 de julio del 2023
El informe técnico sobre el H5N1 más reciente está disponible en la página web de informes técnicos sobre el H5N1.
Resumen ejecutivo
A pesar de la naturaleza panzoótica de los virus de la influenza aviar A(H5N1) altamente patógena (HPAI) en aves silvestres y aves de corral, desde el 2022 solo se ha identificado una cantidad mínima de casos esporádicos del virus de influenza A(H5N1) en seres humanos. Prácticamente todos los casos en seres humanos notificados desde el 2022 estuvieron asociados a exposiciones recientes a aves de corral, y no se han identificado casos de contagio entre personas o de mamíferos a personas del virus A(H5N1) de la HPAI. En algunos casos se desconoce la fuente de exposición al virus A(H5N1) de la HPAI. A la fecha, los virus A(H5N1) HPAI en circulación en aves y aves de corral con derrame a mamíferos, y aquellos que han causado infecciones en seres humanos, no tienen la capacidad de fijarse fácilmente a los receptores que predominan en las vías respiratorias superiores de los seres humanos. Por consiguiente, el riesgo actual para el público de los virus A(H5N1) de la forma altamente patógena de la influenza aviar sigue siendo bajo. Sin embargo, debido a la prevalencia global de brotes de los virus A(H5N1) de la forma altamente patógena de la influenza aviar en brotes en aves silvestres y aves de corral, se anticipa que continúen los casos esporádicos de infecciones en humanos. Si bien los brotes en las bandadas de aves en los EE. UU. han disminuido considerablemente durante los meses de primavera y verano, la circulación a nivel mundial en curso de los virus A(H5N1) de la HPAI en aves silvestres, y su capacidad para propagarse a lo largo de las rutas migratorias y evolucionar rápidamente justifican una vigilancia exhaustiva de estos virus en aves silvestres, aves de corral, mamíferos y personas en todo el mundo, y las reevaluaciones frecuentes para determinar el riesgo para la salud pública, junto con esfuerzos de preparación constantes.
- Los CDC están trabajando activamente en las situaciones en el país que involucran virus A(H5N1) de la HPAI del clado 2.3.4.4b asociadas a infecciones en brotes en aves silvestres y aves de corral, lo que incluye la vigilancia entre las personas con exposiciones relevantes y la preparación ante la posibilidad de que los virus A(H5N1) de la HPAI desarrollen la capacidad de mayor transmisibilidad a las personas.
- Los CDC, junto con sus socios de salud pública estatales y locales, siguen monitoreando activamente a las personas en los Estados Unidos que estuvieron expuestas a aves de corral y aves infectadas por 10 días después de la exposición. A la fecha, se ha monitoreado a más de 6 500 personas en 52 jurisdicciones desde el 2022, y solo se ha identificado un caso en seres humanos.
- Ya está disponible un virus H5 de vacuna experimental (CVV, por sus siglas en inglés) producido por los CDC que se espera que ofrezca buena protección contra los virus A(H5N1) de la HPAI del clado 2.3.4.4b detectados en aves y mamíferos, y ha sido compartido con los fabricantes de vacunas.
- Como los virus de la influenza cambian constantemente, los CDC realizan análisis constantes de los virus A(H5N1) de la HPAI para identificar cambios que podrían propiciar una propagación más fácil entre las personas, causar una enfermedad grave en las personas, reducir la susceptibilidad a los antivirales, afectar la sensibilidad de las pruebas de diagnóstico o reducir el efecto de neutralización de los virus por parte de los anticuerpos inducidos por vacunas. A la fecha se han identificado pocos cambios en los virus A(H5N1) de la HPAI que sean de preocupación para la salud pública, y dichos cambios han variado entre los diversos virus A(H5N1) de la HPAI que circulan en aves silvestres y aves de corral de todo el mundo o que han provocado infecciones esporádicas en seres humanos. No se han identificado cambios en los virus actuales A(H5N1) de la HPAI del clado 2.3.4.4b en aves silvestres, aves de corral, mamíferos o casos en seres humanos que sugieran una mayor transmisibilidad a los humanos.
- En la actualidad, se cree que los virus A(H5N1) de la HPAI que circulan entre las aves representan un riesgo bajo para la salud del público en general en los Estados Unidos; sin embargo, las personas con exposición a aves infectadas relacionada con su trabajo o con actividades recreativas podrían tener mayor riesgo de infección y deberían adoptar las precauciones correspondientes que se describen en las guías de los CDC.
- La vigilancia integral y las iniciativas de preparación siguen su curso y los CDC adoptan constantemente medidas de preparación en caso de riesgo para las personas a causa de cambios en los virus A(H5N1) HPAI u otros virus nuevos de la influenza A.
- Virus A(H5N1) de la forma altamente patógena de la influenza aviar en aves silvestres y de corral
- Infecciones por los virus A(H5N1) de la forma altamente patógena de la influenza aviar entre mamíferos
- Casos de A(H5N1) en seres humanos
- Monitoreo activo de personas expuestas al virus A(H5N1) de la forma altamente patógena de la influenza aviar en los Estados Unidos
- Vigilancia de la influenza en los EE. UU. para detectar infecciones en seres humanos con virus nuevos de la influenza A, incluido el virus A(H5N1) de la forma altamente patógena de la influenza aviar
Virus A(H5N1) de la forma altamente patógena de la influenza aviar en aves silvestres y de corral
Desde el 2005, los virus A(H5N1) de la forma altamente patógena de la influenza aviar han atravesado procesos amplios de diversificación genética que incluyeron la formación de cientos de genotipos posteriores a su reagrupación con otros virus A de la influenza aviar. Los virus A(H5N1) del clado 2.3.4.4b de la forma altamente patógena de la influenza aviar aparecieron en el 2020 y llegaron a Norteamérica a fines del 2021 [1,2] para luego propagarse a América Central y Sudamérica, lo que resultó en brotes en aves silvestres y de corral en muchos países [3–5].
Estos virus A(H5N1) del clado 2.3.4.4b de la forma altamente patógena de la influenza aviar se han propagado en todo el mundo causando cantidades récord de brotes en aves silvestres, domésticas, locales y de corral. 77 estados miembro han notificado más de 15 600 brotes en animales por los virus A(H5N1) de la forma altamente patógena de la influenza aviar a la World Organisation for Animal Health desde enero del 2022.
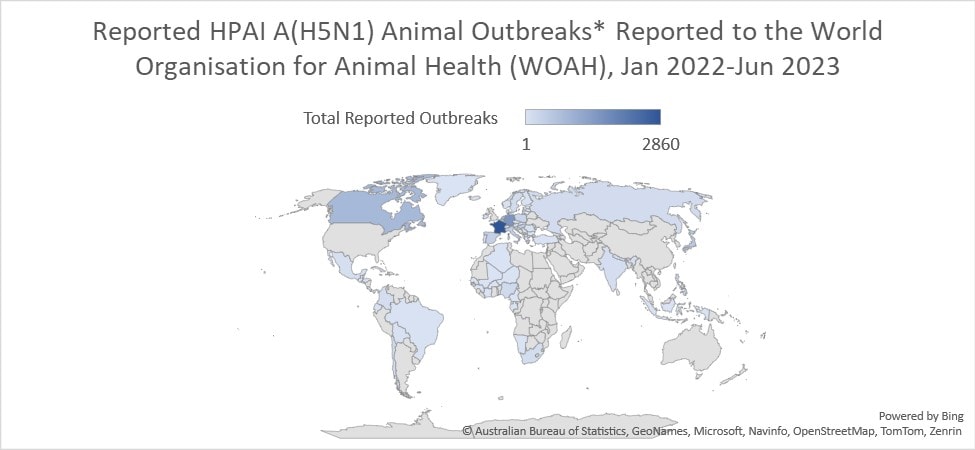
* La WOAH define un brote como la aparición de uno o más casos en un grupo de animales con una relación epidemiológica definida. Por consiguiente, la cantidad de brotes no refleja la cantidad de animales afectados.
En los Estados Unidos, el APHIS del USDA monitorea la aparición de virus de la influenza aviar en aves silvestres, de cría comercial y de corral. Desde enero del 2022 hasta el 27 de junio del 2023, el APHIS notificó detecciones del virus A(H5)/A(H5N1) de la HPAI en más de 7,000 aves silvestres en 50 estados o territorios, y más de 800 bandadas de cría comercial y de corral en 47 estados o territorios. No se han detectado virus A(H5)/A(H5N1) de la HPAI en aves de corral domésticas ni comerciales en los EE. UU. desde el 19 de abril del 2023 y el 18 de mayo del 2023, respectivamente, lo que representa una disminución en comparación con el mismo periodo del 2022.
Infecciones por los virus A(H5N1) de la forma altamente patógena de la influenza aviar entre mamíferos
Se han notificado infecciones esporádicas por el virus A(H5N1) de la HPAI (forma altamente patógena de la influenza aviar) en mamíferos desde el 2003 durante los brotes del virus A(H5N1) de la HPAI en aves de corral o aves silvestres. [6–8]. Se sabe que los virus A(H5) de la HPAI infectan en ocasiones a mamíferos que comen aves o aves de corral (presumiblemente infectadas) o a mamíferos expuestos a entornos con alta concentración del virus.
En los Estados Unidos, entre mayo del 2022 y el 27 de junio del 2023, el APHIS del USDA notificó la detección del virus A(H5N1) de la HPAI en 196 mamíferos de diferentes especies en 26 estados o territorios. En el mundo se han notificado infecciones por el virus A(H5N1) de la HPAI en diversas especies de mamíferos en varios países; por ejemplo, en visones de granja en España, focas grises y de puerto en los Estados Unidos, lobos marinos de Perú y Chile, un gato en Francia y otros países, y zorros en Norteamérica y Europa [9]. Los informes de infecciones por el virus A(H5N1) de la HPAI en mamíferos no sorprenden dados los brotes generalizados de infecciones por el virus A(H5N1) de la HPAI en aves silvestres.
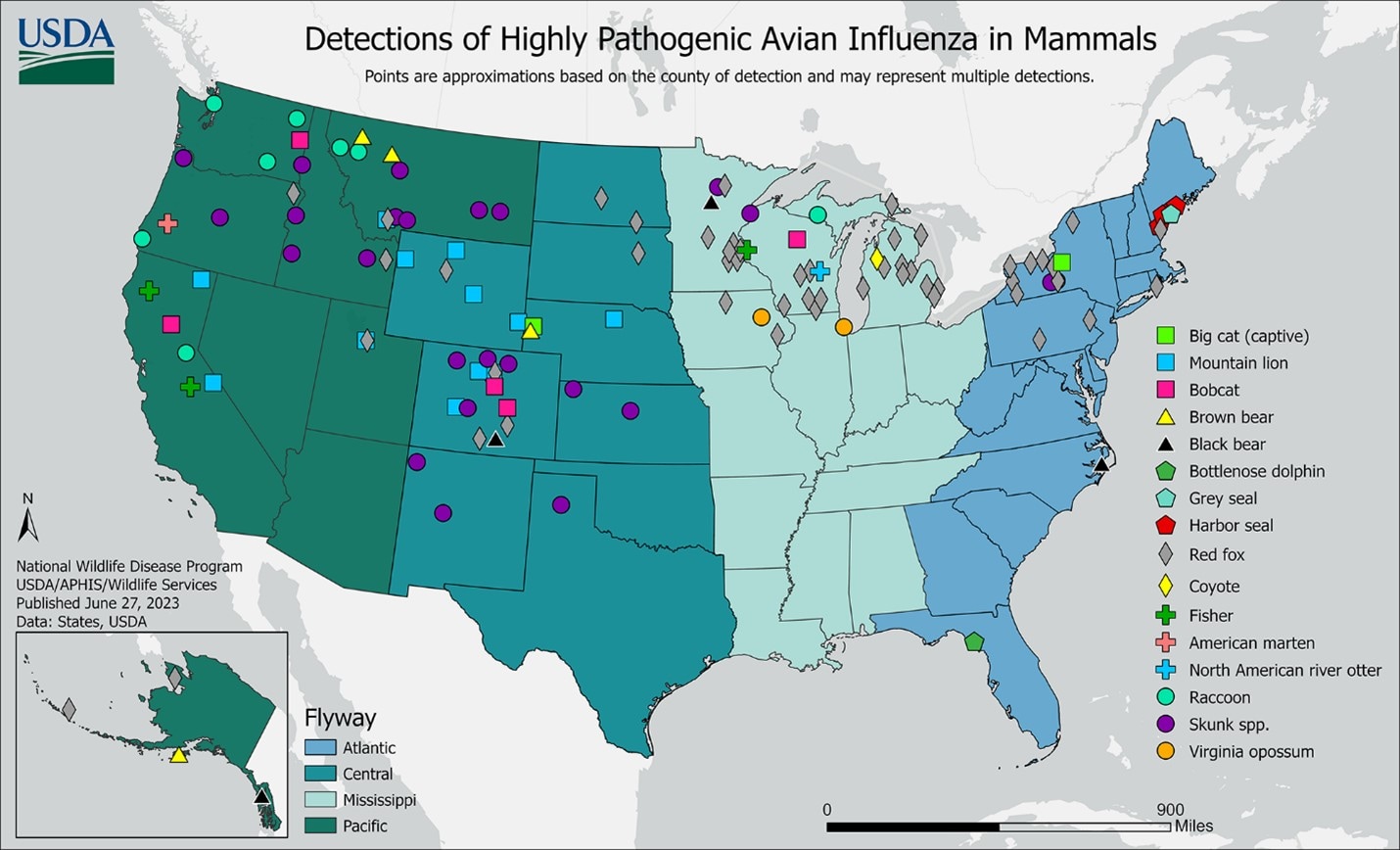
Fuente: APHIS del USDA | Detección de la forma altamente patógena de la influenza aviar en mamíferos en 2022-2023
Los datos genéticos han revelado que cuando algunos mamíferos se infectan por el virus A(H5N1) de la forma altamente patógena de la influenza aviar, el virus puede atravesar un proceso de evolución en su huésped, lo que resulta en cambios genéticos que le permiten al virus replicarse de manera más eficiente en las vías respiratorias inferiores [10-12].
Aunque estos cambios genéticos pueden impactar en las consecuencias de la enfermedad para los mamíferos, no han sido asociados a una especificidad de unión a receptor o a una mayor transmisibilidad del virus a los seres humanos. En la actualidad, los virus A(H5N1) de la forma altamente patógena de la influenza aviar no tienen la capacidad de infectar fácilmente y fijarse a los receptores del ácido siálico en el enlace α2,6, que son los que predominan en las vías respiratorias superiores de los seres humanos [2], lo que sería necesario para aumentar el riesgo de transmisión a las personas [13,14].
Casos de A(H5N1) en seres humanos
Si bien los virus A(H5N1) de la forma altamente patógena de la influenza aviar están en circulación extendida entre aves silvestres y de corral en muchas regiones geográficas, en los últimos años se ha a notificado una cantidad relativamente baja de casos de A(H5N1) en seres humanos [figura 1]. Desde enero del 2022 hasta el 29 de junio del 2023, se notificaron trece casos esporádicos del virus A(H5N1) en seres humanos de ocho países, incluidos seis casos graves y dos muertes, dos casos leves y cinco casos asintomáticos. [Tabla 1].
En los Estados Unidos se notificó un caso de A(H5N1) en un ser humano en abril del 2022. La persona refirió fatiga sin otros síntomas y se detectaron niveles bajos de ARN viral para A(H5N1) en una sola muestra de las vías respiratorias superiores. Es posible que la detección de ARN viral para A(H5N1) resultara de la deposición de material viral no infeccioso en las vías respiratorias superiores de la persona y no representara una infección real, similar a la contaminación ambiental atribuida a los dos casos asintomáticos notificados en trabajadores de una granja de aves de corral en España [15] y además podría explicar la detección del ARN del virus A(H5N1) en otros trabajadores avícolas asintomáticos en el Reino Unido. [16].
Casi todos los casos en seres humanos de infección por el virus A(H5N1) notificados desde el 2022 tenían antecedentes recientes de exposición a aves de corral enfermas o muertas, y no se identificó ningún caso de transmisión del virus A(H5N1) de la HPAI entre personas. Seis casos (3 niños, 3 adultos) se enfermaron gravemente y dos murieron. Diez casos estuvieron asociados a virus A(H5N1) de la HPAI del clado 2.3.4.4b, la HA del clado en un caso en Vietnam no pudo determinarse y dos casos en Camboya estuvieron asociados al clado 2.3.2.1c de los virus A(H5N1) de la HPAI; ninguna de las secuencias genéticas de estos virus A(H5N1) de la HPAI contenía marcadores conocidos de menor susceptibilidad a los medicamentos antivirales para la influenza actualmente recomendados y aprobados por la FDA.
País del caso
País del caso
Mes de aparición de la enfermedad o detección del caso
Mes de aparición de la enfermedad o detección del caso
Gravedad y consecuencias de la enfermedad
Gravedad y consecuencias de la enfermedad
Clado del virus por secuenciación o brotes en aves de corral asociados
Clado del virus por secuenciación o brotes en aves de corral asociados
Camboya
Camboya
Febrero 2023
Febrero 2023
Enfermedad grave, murió
Enfermedad grave, murió
Clado 2.3.2.1c
Clado 2.3.2.1c
Camboya
Camboya
Febrero 2023
Febrero 2023
Enfermedad leve, sobrevivió
Enfermedad leve, sobrevivió
Clado 2.3.2.1c
Clado 2.3.2.1c
Chile*
Chile*
Marzo 2023
Marzo 2023
Enfermedad crítica
Enfermedad crítica
Clado 2.3.4.4b
Clado 2.3.4.4b
China
China
Septiembre 2022
Septiembre 2022
Enfermedad grave, murió
Enfermedad grave, murió
Clado 2.3.4.4b
Clado 2.3.4.4b
China
China
Enero 2023
Enero 2023
Hospitalización, no se notificó resultado final
Hospitalización, no se notificó resultado final
Clado 2.3.4.4b
Clado 2.3.4.4b
Ecuador
Ecuador
Diciembre 2022
Diciembre 2022
Enfermedad grave, sobrevivió
Enfermedad grave, sobrevivió
Clado 2.3.4.4b
Clado 2.3.4.4b
España
España
Septiembre 2022
Septiembre 2022
Asintomático
Asintomático
Clado 2.3.4.4b
Clado 2.3.4.4b
España
España
Octubre 2022
Octubre 2022
Asintomático
Asintomático
Clado 2.3.4.4b
Clado 2.3.4.4b
Reino Unido
Reino Unido
Enero 2022
Enero 2022
Asintomático
Asintomático
Clado 2.3.4.4b
Clado 2.3.4.4b
Reino Unido
Reino Unido
Mayo 2023
Mayo 2023
Asintomático
Asintomático
Clado 2.3.4.4b
Clado 2.3.4.4b
Reino Unido
Reino Unido
Mayo 2023
Mayo 2023
Asintomático
Asintomático
Clado 2.3.4.4b
Clado 2.3.4.4b
Estados Unidos
Estados Unidos
Abril 2022
Abril 2022
Solo fatiga, sobrevivió
Solo fatiga, sobrevivió
Clado 2.3.4.4b
Clado 2.3.4.4b
Vietnam
Vietnam
Octubre 2022
Octubre 2022
Enfermedad grave, sobrevivió
Enfermedad grave, sobrevivió
No informado
No informado
*Hay más detalles sobre el caso/paciente de Chile y las características del virus en: /flu/avianflu/spotlights/2022-2023/chile-first-case-h5n1-addendum.htm
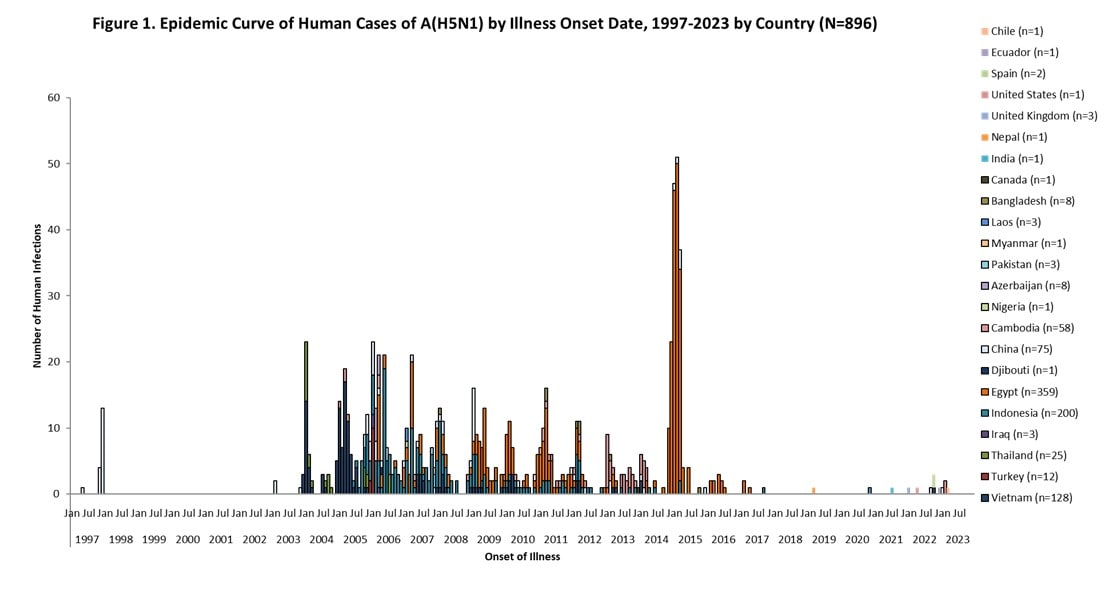
Desde 1997, se ha notificado un total de 896 infecciones esporádicas en seres humanos por el virus A(H5N1) en 22 países [figura 1], causados por diferentes clados del virus A(H5N1) de la forma altamente patógena de la influenza aviar [17], con una proporción de muerte acumulada superior al 50 %. La incidencia anual de casos de infección por el virus A(H5N1) en humanos ha sido mayor en el 2015 (145 casos, 4 países) principalmente debido a una gran epidemia en Egipto con 136 casos, seguidos por el 2006 (115 casos, 9 países) [figura 1].
Casi todos los casos de A(H5N1) en seres humanos notificados estaban asociados a exposiciones a aves de corral enfermas o muertas o a visitas a mercados de aves vivas. Es probable que se hayan producido algunas transmisiones entre personas poco frecuentes, limitadas y no sostenidas del virus de la influenza A(H5N1) de la HPAI en una cantidad reducida de familiares después de la exposición prolongada, estrecha y sin protección con un paciente sintomático durante el 2004-2007 en varios países [18-21].
Monitoreo activo de personas expuestas al virus A(H5N1) de la forma altamente patógena de la influenza aviar en los Estados Unidos
Si bien en el último tiempo hubo algunos casos en seres humanos, dada la extensión de las infecciones entre aves de corral y aves silvestres, las personas con exposición por motivos laborales o recreativos a aves infectadas o a mamíferos enfermos o muertos podrían correr mayor riesgo de infección.
Los CDC, junto con socios de salud pública estatales, territoriales y locales, monitorean de manera activa a las personas expuestas (p. ej., propietarios de bandadas, trabajadores agrícolas y mataderos) a aves de corral comerciales, aves domésticas, aves silvestres y a ambientes con aves infectadas por el virus A(H5N1) de la HPAI durante 10 días después de la última exposición [22]. Al 29 de junio del 2023:
- Total de personas monitoreadas: más de 6 500 en 52 jurisdicciones desde febrero del 2022
- Cantidad total de casos con pruebas de influenza notificadas entre las personas monitoreadas: más de 160 personas
- Cantidad de resultados positivos para el virus de la influenza A(H5N1): 1
De las aproximadamente 160 personas con síntomas a quienes se les realizaron pruebas de detección de virus de la influenza estacional A nuevos, además de otros virus respiratorios, se detectó material genético del virus A(H5N1) de la influenza aviar altamente patógena en una persona de Colorado que refirió fatiga sin ningún otro síntoma al sacrificar aves de corral. [Ver la sección de arriba sobre "Casos de A(H5N1) en seres humanos.”]
Vigilancia de la influenza en los EE. UU. para detectar infecciones en seres humanos con virus nuevos de la influenza A, incluido el virus A(H5N1) de la forma altamente patógena de la influenza aviar
La infección en seres humanos por un virus nuevo de la influenza A, incluido el virus A(H5N1) de la influenza aviar altamente patógena, es una afección de notificación obligatoria a nivel nacional (definición de caso: Definición de caso de infecciones por un virus A de la influenza nuevo, 2014 | CDC)
Hay pruebas de detección de la influenza ampliamente disponibles en laboratorios clínicos y centros de atención médica. Las pruebas en estos entornos permiten detectar infecciones por el virus de la influenza A(H5N1) como positivas para influenza A, y hay un subgrupo de pruebas que también permitirían determinar que no se trata de los subtipos de virus de influenza A (H1 o H3) que suelen circular entre los seres humanos. Las pruebas de personas que pudieron haber estado expuestas al virus H5N1 o que dan positivo para un virus de influenza A pero negativo para los subtipos A(H1) y A(H3) se deben enviar al laboratorio de salud pública estatal o local para un análisis más exhaustivo. Se han enviado muy pocas muestras a los CDC para la realización de pruebas de detección del H5 desde enero del 2022.
- Las pruebas de detección del virus de la influenza estacional que también permiten detectar virus nuevos de influenza A se usan en 128 laboratorios de salud pública de los 50 estados de los EE. UU.
- Hay pruebas de diagnóstico específicas para detectar virus A(H5) actuales en 99 laboratorios de salud pública de los 50 estados.
De conformidad con protocolos estándar de larga data, al detectar un virus positivo para la influenza A, pero negativo para los genes H1 o H3 del virus de influenza humana, el laboratorio de salud pública contactará inmediatamente a los CDC y les enviará la muestra. Las muestras que son positivas para la influenza A pero negativas para los genes H1 o H3 humanos también pueden ser analizadas para H5 por los laboratorios de salud pública estatales y se envían rápidamente a los CDC para obtener un resultado de diagnóstico. Se inicia una investigación del caso y se completa un formulario de notificación de caso que se envía a los CDC a través del módulo de notificación de virus de influenza A nuevos.
Actividad
Actividad
Resumen
Resumen
Vigilancia mundial y respuesta rápida a infecciones en humanos
Vigilancia mundial y respuesta rápida a infecciones en humanos
La División de Influenza de los CDC brinda apoyo a la vigilancia en mercados de aves vivas, granjas domésticas y aves silvestres y/o sus entornos en Bangladesh, Camboya, China, Guatemala, Kenia, Laos, Perú, Tailandia y Vietnam. Los datos de vigilancia señalan la alta prevalencia y amplia variedad de virus A de la influenza aviar en aves y ayudan a describir los cambios en la epidemiología de los virus A de la influenza aviar.
En 2022, la División de Influenza hizo el seguimiento de más de 50 infecciones en seres humanos con los virus A de la influenza aviar notificadas a la OMS por parte de siete países en cuatro regiones de la OMS. En el último tiempo, el personal de campo de la División de Influenza de los CDC colaboró en investigaciones de respuesta rápida de dos casos de H5N1 en seres humanos en Camboya en el 2023..
La División de Influenza de los CDC brinda apoyo a la vigilancia en mercados de aves vivas, granjas domésticas y aves silvestres y/o sus entornos en Bangladesh, Camboya, China, Guatemala, Kenia, Laos, Perú, Tailandia y Vietnam. Los datos de vigilancia señalan la alta prevalencia y amplia variedad de virus A de la influenza aviar en aves y ayudan a describir los cambios en la epidemiología de los virus A de la influenza aviar.
En 2022, la División de Influenza hizo el seguimiento de más de 50 infecciones en seres humanos con los virus A de la influenza aviar notificadas a la OMS por parte de siete países en cuatro regiones de la OMS. En el último tiempo, el personal de campo de la División de Influenza de los CDC colaboró en investigaciones de respuesta rápida de dos casos de H5N1 en seres humanos en Camboya en el 2023..
Evaluaciones virológicas
Evaluaciones virológicas
Como los virus de la influenza tienen altos índices de error durante su replicación y evolucionan rápidamente, los CDC realizan análisis genéticos de manera constante a los virus para identificar cambios que puedan impactar en sus fenotipos, como su antigenicidad, susceptibilidad a los antivirales, transmisibilidad y/o patogénesis. También se analizan genéticamente para evaluar cambios que puedan afectar el rendimiento de las pruebas de diagnóstico.
Como los virus de la influenza tienen altos índices de error durante su replicación y evolucionan rápidamente, los CDC realizan análisis genéticos de manera constante a los virus para identificar cambios que puedan impactar en sus fenotipos, como su antigenicidad, susceptibilidad a los antivirales, transmisibilidad y/o patogénesis. También se analizan genéticamente para evaluar cambios que puedan afectar el rendimiento de las pruebas de diagnóstico.
Diagnóstico
Diagnóstico
Hay diferentes pruebas de diagnóstico de reacción de la cadena de polimerasa en transcripción reversa (RT-PCR, por sus siglas en inglés) en tiempo real de virus de la influenza de los CDC permiten detectar los virus típicos (estacionales) que afectan a los seres humanos o virus nuevos de influenza A (por ejemplo, H5, H7) que pueden infectar a personas por transmisión zoonótica. Estas pruebas de diagnóstico se utilizan en los 50 estados de los EE. UU. y en todo el mundo. Además, existen pruebas de diagnóstico de los CDC que detectan específicamente los virus H5 actuales, las cuales están disponibles en los laboratorios de salud pública en los 50 estados de los EE. UU. y en laboratorios internacionales.
Es probable que la mayoría de las pruebas comerciales utilizadas para la detección de virus de la influenza en seres humanos permitan detectar los virus A(H5N1) de la forma altamente patógena de la influenza aviar porque apuntan a las proteínas conservadas.
Hay diferentes pruebas de diagnóstico de reacción de la cadena de polimerasa en transcripción reversa (RT-PCR, por sus siglas en inglés) en tiempo real de virus de la influenza de los CDC permiten detectar los virus típicos (estacionales) que afectan a los seres humanos o virus nuevos de influenza A (por ejemplo, H5, H7) que pueden infectar a personas por transmisión zoonótica. Estas pruebas de diagnóstico se utilizan en los 50 estados de los EE. UU. y en todo el mundo. Además, existen pruebas de diagnóstico de los CDC que detectan específicamente los virus H5 actuales, las cuales están disponibles en los laboratorios de salud pública en los 50 estados de los EE. UU. y en laboratorios internacionales.
Es probable que la mayoría de las pruebas comerciales utilizadas para la detección de virus de la influenza en seres humanos permitan detectar los virus A(H5N1) de la forma altamente patógena de la influenza aviar porque apuntan a las proteínas conservadas.
Desarrollo de virus de vacuna experimental
Desarrollo de virus de vacuna experimental
El desarrollo de virus de vacuna experimentales (CVV), en coordinación con la OMS, sigue siendo un componente esencial de la estrategia global de preparación para una pandemia de influenza. Se ha creado una biblioteca de virus H5 de vacuna experimental con recomendaciones adicionales para su desarrollo durante las reuniones de consulta bianuales sobre vacunas (Vea la tabla y https://www.who.int/teams/global-influenza-programme/vaccines/who-recommendations/zoonotic-influenza-viruses-and-candidate-vaccine-viruses). La herramienta de evaluación del riesgo de influenza de los CDC también se utiliza para ayudar a priorizar los virus A(H5) de la HPAI para el desarrollo de virus de vacuna experimental.
Se han desarrollado CVV similares al A/Astrakhan/3212/2020 y al A/Silbón americano/Carolina del Sur/22-000345-001/2021, estrechamente relacionados con los virus A(H5N1) (clado 2.3.4.4b) de la HPAI en circulación en América del Norte y están a disposición de los fabricantes de vacunas. Los dos CVV producidos por los CDC (es decir, IDCDC-RG71A) y IDCDC-RG78A) de los EE. UU. y un CVV producido por la FDA (CBER-RG8A) de los EE. UU. codifican una hemaglutinina (HA) que es casi idéntica o idéntica a la HA de los virus H5N1 del clado 2.3.4.4b más recientes detectados en aves y mamíferos, y podrían usarse para producir una vacuna para las personas, si fuera necesario. Se ha recomendado el desarrollo de otros dos CVV H5N1 del clado 2.3.4.4b como parte de la preparación para la pandemia. Además de los CVV para los virus del clado 2.3.4.4b, se han desarrollado CVV para los virus del clado 2.3.2.1c, como los que han infectado a seres humanos en Camboya durante el 2023. Las pruebas antigénicas demuestran que dos CVV del clado 2.3.2.1, NIBRG-301 (A/pato/Vietnam/tipo NCVD-1584/2012) e IDCDC-RG75A (A/pollo/Ghana/tipo 20/2015), ofrecerán protección contra los virus identificados en Camboya en el 2023.
El desarrollo de virus de vacuna experimentales (CVV), en coordinación con la OMS, sigue siendo un componente esencial de la estrategia global de preparación para una pandemia de influenza. Se ha creado una biblioteca de virus H5 de vacuna experimental con recomendaciones adicionales para su desarrollo durante las reuniones de consulta bianuales sobre vacunas (Vea la tabla y https://www.who.int/teams/global-influenza-programme/vaccines/who-recommendations/zoonotic-influenza-viruses-and-candidate-vaccine-viruses). La herramienta de evaluación del riesgo de influenza de los CDC también se utiliza para ayudar a priorizar los virus A(H5) de la HPAI para el desarrollo de virus de vacuna experimental.
Se han desarrollado CVV similares al A/Astrakhan/3212/2020 y al A/Silbón americano/Carolina del Sur/22-000345-001/2021, estrechamente relacionados con los virus A(H5N1) (clado 2.3.4.4b) de la HPAI en circulación en América del Norte y están a disposición de los fabricantes de vacunas. Los dos CVV producidos por los CDC (es decir, IDCDC-RG71A) y IDCDC-RG78A) de los EE. UU. y un CVV producido por la FDA (CBER-RG8A) de los EE. UU. codifican una hemaglutinina (HA) que es casi idéntica o idéntica a la HA de los virus H5N1 del clado 2.3.4.4b más recientes detectados en aves y mamíferos, y podrían usarse para producir una vacuna para las personas, si fuera necesario. Se ha recomendado el desarrollo de otros dos CVV H5N1 del clado 2.3.4.4b como parte de la preparación para la pandemia. Además de los CVV para los virus del clado 2.3.4.4b, se han desarrollado CVV para los virus del clado 2.3.2.1c, como los que han infectado a seres humanos en Camboya durante el 2023. Las pruebas antigénicas demuestran que dos CVV del clado 2.3.2.1, NIBRG-301 (A/pato/Vietnam/tipo NCVD-1584/2012) e IDCDC-RG75A (A/pollo/Ghana/tipo 20/2015), ofrecerán protección contra los virus identificados en Camboya en el 2023.
Vacunas
Vacunas
Las cepas de virus de la influenza con potencial pandémico cambian con el tiempo y hay varias cepas en circulación en animales todos los años sin que esto provoque un contagio entre personas sostenido. El gobierno de los EE. UU. tiene un programa de preparación que permite una respuesta rápida a las cepas del virus de la influenza a medida que las cepas evolucionan. Como parte de este programa, la Autoridad de Investigación y Desarrollo Biomédico de Avanzada (BARDA) trabaja junto a socios de la industria privada para elaborar y analizar pequeñas cantidades de vacunas actualizadas que coincidan con las nuevas cepas de los virus de la influenza con potencial pandémico a medida que aparecen, por si alguno de ellos resulta en contagio sostenido entre personas y al mismo tiempo, sustentar la capacidad de fabricación para propiciar una producción de vacunas a mayor escala cuando sea necesario.
Las cepas de virus de la influenza con potencial pandémico cambian con el tiempo y hay varias cepas en circulación en animales todos los años sin que esto provoque un contagio entre personas sostenido. El gobierno de los EE. UU. tiene un programa de preparación que permite una respuesta rápida a las cepas del virus de la influenza a medida que las cepas evolucionan. Como parte de este programa, la Autoridad de Investigación y Desarrollo Biomédico de Avanzada (BARDA) trabaja junto a socios de la industria privada para elaborar y analizar pequeñas cantidades de vacunas actualizadas que coincidan con las nuevas cepas de los virus de la influenza con potencial pandémico a medida que aparecen, por si alguno de ellos resulta en contagio sostenido entre personas y al mismo tiempo, sustentar la capacidad de fabricación para propiciar una producción de vacunas a mayor escala cuando sea necesario.
Limitaciones del informe
Este informe está sujeto a las siguientes limitaciones. Primero, la cantidad de infecciones en seres humanos por el virus A(H5N1) clado 2.3.4.4b de la influenza aviar altamente patógena es muy reducida. Las conclusiones de los análisis de caracterización de los virus, su transmisibilidad de animales a personas, transmisibilidad entre personas y espectro de presentación clínica de la enfermedad en personas se deben interpretar considerando esta cantidad pequeña. Segundo, no había información detallada de exposiciones disponible para todas las personas monitoreadas en busca de enfermedad después de la exposición a aves y aves de corral infectadas por el virus A(H5N1) de la forma altamente patógena de la influenza aviar en los Estados Unidos. Por consiguiente, no pudimos evaluar el impacto de las variables de exposición como su duración, naturaleza (por ejemplo, contacto directo o indirecto) y el uso de equipos de protección personal sobre el riesgo de infección.
Conclusiones
- A la fecha, los análisis de los virus A(H5N1) de la HPAI del clado 2.3.4.4b realizados por los CDC en aves silvestres, aves de corral y esporádicamente en mamíferos desde fines del 2021 indican que todos estos virus tienen un alto grado de identidad genética entre sí y no se identificó ninguna sustitución adaptativa, inserción ni eliminación en mamíferos significativa, particularmente en el gen de la HA, que es importante para la transmisión zoonótica y el posterior contagio entre personas.
- Considerando la prevalencia alta de los virus A(H5N1) de la forma altamente patógena de la influenza aviar en aves silvestres y de corral en todo el mundo, se prevé el derrame a mamíferos (particularmente, carnívoros que se alimentan de especies aviares infectadas) y otras infecciones zoonóticas esporádicas entre personas con exposición a aves de corral y silvestres enfermas o muertas.
- La HA de los virus A(H5N1) del clado 2.3.4.4b en circulación en la actualidad en aves silvestres y de corral de todo el mundo no tiene la capacidad de fijarse preferencialmente a los tipos de receptores de ácido siálico que predominan en las vías respiratorias superiores de los seres humanos y, por consiguiente, por el momento no tienen la capacidad de infectar o transmitirse fácilmente entre personas.
- A pesar de la propagación mundial de los virus A(H5N1) de la influenza en aves silvestres y aves de corral en los últimos años, se notificó solo una pequeña cantidad de infecciones en humanos por los virus H5N1 de los clados 2.3.4.4b o 2.3.2.1c desde el 2022; todos los casos tenían exposición reciente a aves de corral y no se identificó ningún caso de transmisión del virus A(H5N1) de la influenza entre personas.
Si bien la evaluación de los CDC es que la amenaza general de la HA de los virus A(H5N1) del clado 2.3.4.4b para la salud pública es baja por el momento, la prevalencia de propagación geográfica en aves de corral y aves infectadas eleva la posibilidad de exposiciones de seres humanos y otros mamíferos, lo que podría provocar la evolución del virus y su redistribución y, a su vez, producir un cambio en la evaluación del riesgo actual. Aunque las detecciones de virus en aves de corral comerciales y aves domésticas en los Estados Unidos disminuyeron considerablemente en los últimos meses, la situación podría cambiar en cualquier momento. La vigilancia en curso de los virus A(H5N1) de la forma altamente patógena de la influenza aviar en circulación en aves silvestres, aves de corral e infecciones esporádicas en mamíferos y personas en todo el mundo es crítica para monitorear el riesgo para la salud pública y detectar cambios genéticos (particularmente, en el gen de la HA) que pudieran modificar la evaluación de riesgo de los CDC.
Referencias
- Bevins SN, Shriner SA, Cumbee JC Jr, Dilione KE, Douglass KE, Ellis JW et al. Intercontinental Movement of Highly Pathogenic Avian Influenza A(H5N1) Clade 2.3.4.4 Virus to the United States, 2021. Emerg Infect Dis. 2022 May;28(5):1006-1011. doi: 10.32/eid2805.220318.
- Kandeil A, Patton C, Jones JC, Jeevan T, Harrington WN, Trifkovic S et al. Rapid evolution of A(H5N1) influenza viruses after intercontinental spread to North America. Nat Commun. 2023 May 29;14(1):3082. doi: 10.1/s41467-023-38415-7.
- World Health Organization. Antigenic and genetic characteristics of zoonotic influenza A viruses and development of candidate vaccine viruses for pandemic preparedness. February 2023. https://cdn.who.int/media/docs/default-source/influenza/who-influenza-recommendations/vcm-northern-hemisphere-recommendation-2023-2024/20230224_zoonotic_recommendations.pdf?sfvrsn=38c739fa_4 [1.13 MB, 12 páginas]
- European Food Safety Authority, European Centre for Disease Prevention and Control, European Union Reference Laboratory for Avian Influenza. Avian influenza overview March - April 2023. EFSA J 2023 Jun 7;21(6):e08039. doi: 10.29/j.efsa.2023.8039.
- Food and Agriculture Organization of the United Nations. Global Avian Influenza Viruses with Zoonotic Potential situation update, 22 June 2023. https://www.fao.org/animal-health/situation-updates/global-aiv-with-zoonotic-potential
- Keawcharoen J, Oraveerakul K, Kuiken T, Fouchier RAM, Amonsin A, Payungporn S et al. Avian influenza H5N1 in tigers and leopards. Emerg Infect Dis. 2004 Dec;10(12):2189-91. doi: 10.32/eid1012.040759.
- Songserm T, Amonsin A, Jam-on R, Sae-Heng N, Pariyothorn N, Payungporn S et al. Fatal avian influenza A H5N1 in a dog. Emerg Infect Dis. 2006 Nov;12(11):1744-7. doi: 10.32/eid1211.060542.
- Songserm T, Amonsin A, Jam-on R, Sae-Heng N, Meemak N, Pariyothorn N et al. Avian influenza H5N1 in naturally infected domestic cat. Emerg Infect Dis. 2006 Apr;12(4):681-3. doi: 10.32/eid1204.051396.
- Pan American Health Organization. Epidemiological Update Outbreaks of avian influenza caused by influenza A(H5N1) in the Region of the Americas, 17 May 2023. epiupdate-avianflu-may-2023-v2.pdf.
- Gabriel G, Czudai-Matwich V, Klenk HD. Adaptive mutations in the H5N1 polymerase complex. Virus Res. 2013 Dec 5;178(1):53-62. doi: 10.1/j.virusres.2013.05.010.
- Bogs J, Kalthoff D, Veits J, Pavlova S, Schwemmle M, Mänz B et al. Reversion of PB2-627E to -627K during replication of an H5N1 Clade 2.2 virus in mammalian hosts depends on the origin of the nucleoprotein. J Virol. 2011 Oct;85(20):10691-8. doi: 10.11/JVI.00786-11.
- Agüero M, Monne I, Sánchez A, Zecchin B, Fusaro A, Ruano MJ et al. Highly pathogenic avian influenza A(H5N1) virus infection in farmed minks, Spain, October 2022. Euro Surveill. 2023 Jan;28(3):2300001. doi: 10.28/1560-7917.ES.2023.28.3.2300001.
- van Riel D, den Bakker MA, Leijten LM, Chutinimitkul S, Munster VJ, de Wit E et al. Seasonal and pandemic human influenza viruses attach better to human upper respiratory tract epithelium than avian influenza viruses. Am J Pathol. 2010 Apr;176(4):1614-8. doi: 10.24/ajpath.2010.090949.
- Shinya K, Ebina M, Yamada S, Ono M, Kasai N, Kawaoka Y. Avian flu: influenza virus receptors in the human airway. Nature. 2006 Mar 23;440(7083):435-6. doi: 10.1/440435a.
- Aznar E, Casas I, González Praetorius A, Ruano Ramos MJ, Pozo F, Sierra Moros MJ et al.Influenza A(H5N1) detection in two asymptomatic poultry farm workers in Spain, September to October 2022: suspected environmental contamination. Euro Surveill. 2023 Feb;28(8):2300107. doi: 10.28/1560-7917.ES.2023.28.8.2300107. https://pubmed.ncbi.nlm.nih.gov/36820643/
- Organización Mundial de la Salud. Avian Influenza A(H5N1) - United Kingdom of Great Britain and Northern Ireland. 30 May 2023. Accessed at: https://www.who.int/emergencies/disease-outbreak-news/item/2023-DON468
- Lai S, Qin Y, Cowling BJ, Ren X, Wardrop NA, Gilbert M et al. Global epidemiology of avian influenza A H5N1 virus infection in humans, 1997-2015: a systematic review of individual case data. Lancet Infect Dis. 2016 Jul;16(7):e108-e118. doi: 10.1/S1473-3099(16)00153-5.
- Ungchusak K, Auewarakul P, Dowell SF, Kitphati R, Auwanit W, Puthavathana P et al. Probable person-to-person transmission of avian influenza A (H5N1). N Engl J Med. 2005 Jan 27;352(4):333-40. doi: 10.11/NEJMoa044021.
- Wang H, Feng Z, Shu Y, Yu H, Zhou L, Zu R et al. Probable limited person-to-person transmission of highly pathogenic avian influenza A (H5N1) virus in China. Lancet. 2008 Apr 26;371(9622):1427-34. doi: 10.1/S0140-6736(08)60493-6.
- WHO Disease Outbreak News. 2006 - Indonesia. 31 May 2006. Accessed at: https://www.who.int/emergencies/disease-outbreak-news/item/2006_05_31-en
- Organización Mundial de la Salud. Human cases of avian influenza A (H5N1) in North-West Frontier Province, Pakistan, October-November 2007. Wkly Epidemiol Rec. 2008 Oct 3;83(40):359-64. Accessed at: https://reliefweb.int/report/guinea/weekly-epidemiological-record-wer-3-october-2008-vol-83-no-40-pp-357-364-enfr
- Kniss K, Sumner KM, Tastad KJ, Lewis NM, Jansen L, Julian D et al. Risk for Infection in Humans after Exposure to Birds Infected with Highly Pathogenic Avian Influenza A(H5N1) Virus, United States, 2022. Emerg Infect Dis. 2023 Jun;29(6):1215-1219. doi: 3201/eid2906.230103.
- Informe técnico: Virus de la influenza aviar A(H5N1) altamente patógena (cdc.gov) - 27 de octubre del 2023
- Informe técnico: Virus de la influenza aviar A(H5N1) altamente patógena (cdc.gov) - 5 de octubre del 2023
- Informe técnico: Virus de la influenza aviar A(H5N1) altamente patógena (cdc.gov) - 7 de julio del 2023
- Anexo: Infección en seres humanos por el virus A(H5N1) de la influenza aviar altamente patógena en Chile (cdc.gov) - 17 de abril del 2023
- Informe técnico: Virus de la influenza aviar A(H5N1) altamente patógena (cdc.gov) - 17 de marzo del 2023
Resumen de situación actual de la influenza aviar | Influenza aviar (gripe aviar) (cdc.gov)
Infecciones por el nuevo virus de influenza A (cdc.gov): panel interactivo de todas las infecciones por el nuevo virus de influenza A en seres humanos notificadas en los Estados Unidos desde el 2010
Infecciones notificadas en humanos por virus de la influenza aviar A
Aspectos destacados de la cronología de la historia de la influenza aviar - 2020 a 2023
Información para personas expuestas a aves infectadas por los virus de la influenza aviar
Las referencias a los sitios no pertenecientes a los CDC se ofrecen como servicio y no constituyen ni implican el respaldo de estas organizaciones o de sus programas por parte de los CDC o el Departamento de Salud y Servicios Humanos de los EE. UU. Los CDC no son responsables por el contenido de las páginas de estos sitios. Las direcciones URL mencionadas estaban actualizadas a la fecha de publicación.
Descargo de responsabilidad: Es posible que en este sitio encuentre algunos enlaces que le lleven a contenido disponible sólo en inglés. Además, el contenido que se ha traducido del inglés se actualiza a menudo, lo cual puede causar la aparición temporal de algunas partes en ese idioma hasta que se termine de traducir (generalmente en 24 horas). Llame al 1-800-CDC-INFO si tiene preguntas sobre la influenza estacional, cuyas respuestas no ha encontrado en este sitio. Agradecemos su paciencia.
